ΤΟΠΙΚΑ ΝΕΑ
Πώς αναπτύσσονται, εγκρίνονται και διατίθενται τα εμβόλια στην αγορά;
Δημοσιεύθηκε
5 έτη πρινστις
Από
Admin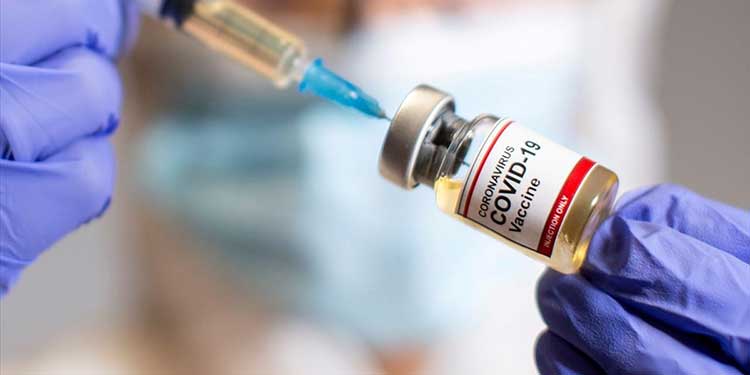
Έγκριση των εμβολίων στην ΕΕ
Λόγω του επείγοντος χαρακτήρα της πανδημίας, τα εμβόλια κατά της COVID-19 αναπτύσσονται και εγκρίνονται ταχύτερα απ’ ό,τι συνήθως. Ωστόσο, θα πληρούν τα ίδια υψηλά πρότυπα με όλα τα άλλα εμβόλια.
Πώς αναπτύχθηκαν τόσο γρήγορα τα εμβόλια κατά της νόσου COVID-19;
 Σημαντικά κεφάλαια έχουν επενδυθεί στην ταχεία ανάπτυξη εμβολίων κατά της COVID-19. Σημαντικά κεφάλαια έχουν επενδυθεί στην ταχεία ανάπτυξη εμβολίων κατά της COVID-19. |
 Οι επιστήμονες κατάφεραν να επιταχύνουν ορισμένα στάδια της διαδικασίας,, συνδυάζοντας διάφορες φάσεις των κλινικών δοκιμών ή διενεργώντας ταυτόχρονα ορισμένες μελέτες. Ο Ευρωπαϊκός Οργανισμός Φαρμάκων ξεκίνησε να ελέγχει τα δεδομένα που προέκυπταν πριν να υποβάλουν αίτηση οι εταιρείες για την έγκριση των εμβολίων τους. Οι επιστήμονες κατάφεραν να επιταχύνουν ορισμένα στάδια της διαδικασίας,, συνδυάζοντας διάφορες φάσεις των κλινικών δοκιμών ή διενεργώντας ταυτόχρονα ορισμένες μελέτες. Ο Ευρωπαϊκός Οργανισμός Φαρμάκων ξεκίνησε να ελέγχει τα δεδομένα που προέκυπταν πριν να υποβάλουν αίτηση οι εταιρείες για την έγκριση των εμβολίων τους. |
 Ορισμένα εμβόλια κατά της COVID-19 αναπτύχθηκαν με τις ίδιες μεθόδους που έχουν χρησιμοποιηθεί για άλλα εμβόλια. Αυτό σημαίνει ότι θα είναι ευκολότερη η χρήση των υφιστάμενων εγκαταστάσεων για τη μαζική παραγωγή εμβολίων κατά της νόσου COVID-19. Ορισμένα εμβόλια κατά της COVID-19 αναπτύχθηκαν με τις ίδιες μεθόδους που έχουν χρησιμοποιηθεί για άλλα εμβόλια. Αυτό σημαίνει ότι θα είναι ευκολότερη η χρήση των υφιστάμενων εγκαταστάσεων για τη μαζική παραγωγή εμβολίων κατά της νόσου COVID-19. |
 Ορισμένα εμβόλια κατά της COVID-19 αναπτύχθηκαν με τη χρήση νέων μεθόδων που μπορούν να αυξήσουν τον όγκο και την ταχύτητα παραγωγής σε σύγκριση με άλλους τύπους εμβολίων. Ορισμένα εμβόλια κατά της COVID-19 αναπτύχθηκαν με τη χρήση νέων μεθόδων που μπορούν να αυξήσουν τον όγκο και την ταχύτητα παραγωγής σε σύγκριση με άλλους τύπους εμβολίων. |
|
Οι εταιρείες ενισχύουν την ικανότητά τους να παράγουν γρήγορα εκατομμύρια δόσεις εγκεκριμένων εμβολίων κατά της COVID-19. |
|
Έγκριση των εμβολίων στην ΕΕ
 |
Όπως όλα τα φάρμακα, τα εμβόλια δοκιμάζονται πρώτα στο εργαστήριο. |
 |
Στη συνέχεια, δοκιμάζονται σε ανθρώπους-εθελοντές σε διάφορους γύρους μελετών που ονομάζονται κλινικές δοκιμές. |
 |
Οι εν λόγω δοκιμές βοηθούν στην επιβεβαίωση του τρόπου με τον οποίο λειτουργούν τα εμβόλια και διασφαλίζουν ότι τα οφέλη τους υπερτερούν των πιθανών παρενεργειών ή κινδύνων. |
 |
Όταν υπάρχουν επαρκή δεδομένα από έρευνες και κλινικές δοκιμές, οι εταιρείες μπορούν να υποβάλουν αίτηση στον Ευρωπαϊκό Οργανισμό Φαρμάκων για τη χορήγηση άδειας κυκλοφορίας του εμβολίου στην αγορά. |
 |
Ο Ευρωπαϊκός Οργανισμός Φαρμάκων εξετάζει όλα τα δεδομένα και διενεργεί ανεξάρτητη και διεξοδική επιστημονική αξιολόγηση του εμβολίου. |
 |
Με βάση την επιστημονική αξιολόγηση του Οργανισμού, η Ευρωπαϊκή Επιτροπή χορηγεί άδεια κυκλοφορίας στην αγορά της ΕΕ. Τότε το εμβόλιο μπορεί να χρησιμοποιηθεί. |
Εμβόλια κατά της νόσου COVID-19
| Εταιρεία | Τύπος εμβολίου | Αριθμός δόσεων
(που απαιτούνται ανά άτομο) |
Αριθμός δόσεων
(που έχουν εξασφαλιστεί στην ΕΕ) |
Κατάσταση |
|---|---|---|---|---|
| BioNTech και Pfizer | mRNA | 2 δόσεις | 600 εκατομμύρια | Εγκρίθηκε |
| Moderna | mRNA | 2 δόσεις | 460 εκατομμύρια | Εγκρίθηκε |
| CureVac | mRNA | 2 δόσεις | 405 εκατομμύρια | Ανάπτυξη υπό εξέλιξη |
| AstraZeneca | αδενοϊός | 2 δόσεις | 400 εκατομμύρια | Εγκρίθηκε |
| Johnson & Johnson/Janssen Pharmaceuticals | αδενοϊός | 1 δόση | 400 εκατομμύρια | Εγκρίθηκε |
| Sanofi-GSK | πρωτεΐνη | 2 δόσεις | 300 εκατομμύρια | Ανάπτυξη υπό εξέλιξη |
Ποιο εμβόλιο έχει ήδη εγκριθεί;
Μετά από θετική αξιολόγηση του Ευρωπαϊκού Οργανισμού Φαρμάκων (EMA) όσον αφορά την ασφάλεια, την ποιότητα και την αποτελεσματικότητά τους, η Επιτροπή έχει μέχρι στιγμής χορηγήσει άδεια κυκλοφορίας υπό όρους για 4 εμβόλια που ανέπτυξαν οι εταιρείες:
- BioNTech and Pfizer, στις 21 Δεκεμβρίου
- Moderna, στις 6 Ιανουαρίου
- AstraZeneca, στις 29 Ιανουαρίου
- Janssen Pharmaceutica NV, στις 11 Μαρτίου
Ποια πιθανά εμβόλια εξετάζει επί του παρόντος ο EMA;
Ο EMA ξεκίνησε κυλιόμενες επανεξετάσεις των εμβολίων κατά της COVID-19 που ανέπτυξαν η Novavax, στις 3 Φεβρουαρίου 2021, και η CureVac AG, στις 12 Φεβρουαρίου 2021, καθώς και του εμβολίου Sputnik V, στις 4 Μαρτίου 2021. Αυτές οι κυλιόμενες επανεξετάσεις θα συνεχιστούν έως ότου υπάρξουν επαρκή αποδεικτικά στοιχεία ώστε να υποβληθεί επίσημη αίτηση χορήγησης άδειας κυκλοφορίας.
Με ποιες εταιρείες έχει συνάψει η Επιτροπή συμφωνίες για εμβόλια;
Η Επιτροπή διεξάγει εντατικές διαπραγματεύσεις προκειμένου να εξασφαλίσει ένα διαφοροποιημένο χαρτοφυλάκιο εμβολίων για τους πολίτες της ΕΕ σε δίκαιες τιμές. Έχουν συναφθεί συμφωνίες με τις εταιρείες AstraZeneca (400 εκατομμύρια δόσεις), Sanofi-GSK (300 εκατομμύρια δόσεις), Johnson and Johnson (400 εκατομμύρια δόσεις), BioNTech-Pfizer (600 εκατομμύρια δόσεις), CureVac (405 εκατομμύρια δόσεις) και Moderna (460 εκατομμύρια δόσεις). Η Επιτροπή ολοκλήρωσε διερευνητικές συνομιλίες με τη φαρμακευτική εταιρεία Novavax με σκοπό την αγορά έως 200 εκατ. δόσεων και με την Valneva με σκοπό την αγορά έως και 60 εκατ. δόσεων.
Άδεια κυκλοφορίας υπό όρους
Σε περίπτωση κατάστασης έκτακτης ανάγκης στον τομέα της δημόσιας υγείας, μπορεί να χορηγηθεί άδεια κυκλοφορίας υπό όρους για ένα φάρμακο ή εμβόλιο.
Αυτό μπορεί να συμβεί όταν το όφελος από την άμεση παροχή του αντισταθμίζει τον κίνδυνο ύπαρξης λιγότερο ολοκληρωμένων δεδομένων από αυτά που απαιτούνται συνήθως. Σ’ αυτές τις περιπτώσεις, ο παρασκευαστής δεσμεύεται να παράσχει πρόσθετες πληροφορίες σύμφωνα με προκαθορισμένο χρονοδιάγραμμα.
Σε κάθε περίπτωση, η Ευρωπαϊκή Επιτροπή θα χορηγήσει άδεια κυκλοφορίας μόνο εάν η αξιολόγηση του Ευρωπαϊκού Οργανισμού Φαρμάκων δείξει ότι το εμβόλιο είναι ταυτόχρονα ασφαλές και αποτελεσματικό.
Ασφάλεια και αποτελεσματικότητα των εμβολίων
Η ασφάλεια και η αποτελεσματικότητα των εμβολίων που έχουν λάβει άδεια κυκλοφορίας υπό όρους παρακολουθούνται αυστηρά, όπως ισχύει για όλα τα φάρμακα, μέσω του θεσπισμένου συστήματος παρακολούθησης φαρμάκων της ΕΕ.
Επιπλέον, λαμβάνονται ειδικά μέτρα για τη γρήγορη συλλογή και αξιολόγηση νέων πληροφοριών. Για παράδειγμα, οι παρασκευαστές πρέπει συνήθως να αποστέλλουν κάθε έξι μήνες έκθεση ασφάλειας στον Ευρωπαϊκό Οργανισμό Φαρμάκων. Ωστόσο, για τα εμβόλια κατά της COVID-19 οι εκθέσεις ασφάλειας πρέπει να αποστέλλονται κάθε μήνα.
Ο Ευρωπαϊκός Οργανισμός Φαρμάκων θα θέσει σε εφαρμογή πρόσθετη παρακολούθηση μεγάλης κλίμακας όσον αφορά την ασφάλεια, δεδομένου του εξαιρετικά υψηλού αριθμού ατόμων που αναμένεται να εμβολιαστούν.
Εκστρατείες εμβολιασμού
Στη συνέχεια, οι εταιρείες παρασκευάζουν τα εγκεκριμένα εμβόλια σε μεγάλη κλίμακα. Η ποσότητα εμβολίων που λαμβάνει κάθε χώρα υπολογίζεται συνήθως με βάση τον πληθυσμό της.
Οι πολίτες μπορούν να εμβολιάζονται σύμφωνα με τα εθνικά προγράμματα εμβολιασμού. Τα εθνικά προγράμματα δίνουν συνήθως προτεραιότητα σε συγκεκριμένες ομάδες, όπως οι επαγγελματίες του τομέα της υγείας και οι ευπαθείς ομάδες (ηλικιωμένοι ή άτομα με υποκείμενα νοσήματα).
Η Επιτροπή στηρίζει τις χώρες της ΕΕ κατά την προετοιμασία και την υλοποίηση των εκστρατειών εμβολιασμού τους.
Πηγή: Επίσημος ιστότοπος της Ευρωπαϊκής Ένωσης
Μπορεί να σας ενδιαφέρουν
-


Αποτελέσματα εκλογών ΣΥΡΙΖΑ στον νομό Δράμας
-


Επαφές του Γιώργου Παπαδόπουλου και υποψηφίων της Επανεκκίνησης
-


“Μαζί για την Αλλαγή” Παρουσίαση υποψηφίων στη Δράμα
-


“Project για τη Δράμα”: Πόσες ψήφους αξίζει ένα εμβόλιο;
-


Ενίσχυση της αυτοεικόνας και προσωπική ενδυνάμωση
-


2ο Γαστρονομικό Φεστιβάλ Δράμας
ΤΟΠΙΚΑ ΝΕΑ
Διανομή τροφίμων από το Κοινωνικό Παντοπωλείο του Δήμου Δράμας
Δημοσιεύθηκε
3 μήνες πρινστις
10 Σεπτεμβρίου 2025Από
GoDrama
Στο πλαίσιο υλοποίησης του προγράμματος διανομών του Καταστήματος Κοινωνικής Αλληλεγγύης (Κοινωνικό Παντοπωλείο) του Δήμου Δράμας από την Δευτέρα 15 Σεπτεμβρίου έως και την Παρασκευή 19 Σεπτεμβρίου 2025 θα πραγματοποιηθεί διανομή στις 479 οικογένειες – δικαιούχους του.
Τα είδη που θα διανεμηθούν στους δικαιούχους είναι τα εξής:
Εξαιρετικά παρθένο ελαιόλαδο 5lt, ηλιέλαιο 5lt, ζάχαρη, αλάτι, αλεύρι, κριθαράκι, ρύζι, μακαρόνια, φακές, φασόλια, γάλα εβαπορέ, ντοματοχυμός, μέλι, χυμός πορτοκάλι, πραλίνα φουντουκιού, μαρμελάδα, φρυγανιές, άνθος αραβοσίτου, κονσέρβα ζαμπόν, κονσέρβα σαρδέλα και τραχανάς.
Παρακαλούνται οι δικαιούχοι να προσέρχονται με την προσωπική τους κάρτα και την ταυτότητα τους αυστηρά την ημέρα και ώρα που είναι καταγεγραμμένη στην προσωπική τους κάρτα.
ΤΟΠΙΚΑ ΝΕΑ
Χριστουγεννιάτικη Αγορά Ονειρούπολης Δήμου Δράμας – Οδηγίες Συμμετοχής
Δημοσιεύθηκε
3 μήνες πρινστις
7 Σεπτεμβρίου 2025Από
GoDrama
Ο Δήμος Δράμας ενημερώνει τους ενδιαφερόμενους πωλητές για τη διαδικασία συμμετοχής στη Χριστουγεννιάτικη Αγορά της Ονειρούπολης, σύμφωνα με τις διατάξεις του ν. 4849/2021.
Δικαίωμα συμμετοχής έχουν οι κάτοχοι:
- Βεβαίωσης δραστηριοποίησης ετήσιας διάρκειας σε βραχυχρόνιες αγορές
- Άδειας πωλητών λαϊκών αγορών
- Άδειας δραστηριοποίησης στο υπαίθριο εμπόριο (στάσιμο ή πλανόδιο)
- Άδειας χειροτέχνη – καλλιτέχνη
Διαδικασία
- Έκδοση προκήρυξης: Η προκήρυξη αναρτάται στο Ολοκληρωμένο Πληροφοριακό Σύστημα «Ανοικτή Αγορά» – OPENMARKET (openmarket.mindev.gov.gr) και στη σελίδα του Δήμου. Εκεί θα δημοσιευθούν ο Κανονισμός Λειτουργίας, έντυπο οδηγιών και υποδείγματα αιτήσεων.
- Υποβολή αιτήσεων: Γίνεται αποκλειστικά ψηφιακά στο OPENMARKET με χρήση κωδικών Taxisnet. Οι ενδιαφερόμενοι υποβάλλουν τη βεβαίωση ή την άδεια που κατέχουν, μαζί με τα απαιτούμενα δικαιολογητικά.
- Αποτελέσματα:
- Εκδίδονται προσωρινά αποτελέσματα, με δυνατότητα υποβολής ενστάσεων εντός 15 ημερών.
- Εκδίδονται τα οριστικά αποτελέσματα, τα οποία εγκρίνονται από το Δημοτικό Συμβούλιο μετά από γνωμοδότηση της τριμελούς επιτροπής.
- Έγκριση και απόδοση θέσεων: Οι δικαιούχοι λαμβάνουν έγκριση συμμετοχής και θέση στη Χριστουγεννιάτικη Αγορά. Η πράξη κοινοποιείται στα αρμόδια ελεγκτικά όργανα και στη Δ.Ο.Υ. Δράμας.
Υποχρεώσεις πωλητών
- Οι άδειες και βεβαιώσεις πρέπει να είναι σε ισχύ και να περιλαμβάνουν σχετικό ΚΑΔ.
- Πριν τη χορήγηση της έγκρισης συμμετοχής απαιτείται η καταβολή του καθορισμένου τέλους στον Δήμο Δράμας (Ταμείο, τράπεζα ή e-banking).
- Οι πωλητές είναι αποκλειστικά υπεύθυνοι για την τήρηση όλων των αγορανομικών, φορολογικών και υγειονομικών διατάξεων.
- Επιτρέπεται υποβοήθηση/αναπλήρωση ή πρόσληψη υπαλλήλου με σχετική βεβαίωση, εκτός των χειροτεχνών – καλλιτεχνών.
- Κάθε ενδιαφερόμενος μπορεί να υποβάλει μία μόνο αίτηση με τον ίδιο ΑΦΜ και σε μία κατηγορία πώλησης.
- Σε περίπτωση μη επιθυμίας συμμετοχής, ο δικαιούχος οφείλει να το δηλώσει εγγράφως στην αρμόδια υπηρεσία.
Πληροφορίες
Οι ενδιαφερόμενοι μπορούν να απευθύνονται στο Αυτοτελές Τμήμα Τοπικής Οικονομικής Ανάπτυξης του Δήμου Δράμας.
Τηλέφωνα: 25213 50686 – 687 – 689
ΤΟΠΙΚΑ ΝΕΑ
Πολλοί υπουργοί αγαπούν περισσότερο την καρέκλα της εξουσίας
Δημοσιεύθηκε
5 μήνες πρινστις
13 Ιουλίου 2025Από
GoDrama
Αναζήτηση στην Google
Αναζήτηση στο GoDrama



Κοινωνικό Φροντιστήριο από Δήμο Δράμας και Φροντιστήρια Μέσης Εκπαίδευσης και Ξένων Γλωσσών
Διανομή τροφίμων από το Κοινωνικό Παντοπωλείο του Δήμου Δράμας

Χριστουγεννιάτικη Αγορά Ονειρούπολης Δήμου Δράμας – Οδηγίες Συμμετοχής

Η Δράμα στο ευρωπαϊκό προσκήνιο της εκπαίδευσης

Πολλοί υπουργοί αγαπούν περισσότερο την καρέκλα της εξουσίας

Θετικό πρόσημο για τον Δήμο Δράμας στη διαχείριση των αδέσποτων

ΟΠΕΚΕΠΕ Το φωνάζαμε εγκαίρως πριν το σκάνδαλο

Το επιχειρηματικό ESG όπως το διαμορφώνει πλέον το πακέτο Omnibus

Απαγόρευση διέλευσης, παραμονής και κυκλοφορίας εντός δασών

KAOD BC: Παρουσίαση του νέου προπονητή Κώστα Σδράκα

Τουρνουά Beach Volley DRAMA OPEN 20-22 Ιουνίου

Παρουσίαση των τουριστικών πλεονεκτημάτων της Δράμας, στο Βελιγράδι
Σεισμός 5,3 Ρίχτερ στη Χαλκιδική

Πανδραμινό Συλλαλητήριο Πέμπτη 12/6 στις 20:00 στην Κεντρική Πλατεία